NO2 + O2 + H2O → HNO3 là phản ứng hóa học, được Trường Cao đẳng nghề Thừa Thiên Huế biên soạn, đối với phương trình Hóa học nhiều bạn học sinh còn lúng túng không biết NO2 tạo ra HNO3 bằng cách nào, dưới đây Trường Cao đẳng nghề Thừa Thiên Huế đã biên soạn, cân bằng phương trình đầy đủ kèm bài tập củng cố đi kèm.
Hy vọng có thể giúp các bạn viết và cân bằng phương trình một cách nhanh và chính xác hơn.
1. Phương trình phản ứng NO2 ra HNO3
4NO2 + O2 + 2H2O → 4HNO3
2. Điều kiện để NO2 ra HNO3
Không có
3. Cách tiến hành phản ứng để NO2 ra HNO3
Cho NO2 tác dụng với O2 và hơi nước trong không khí
4. Hiện tượng phản ứng hóa học xảy ra
Khi cho NO2 tác dụng với O2 và hơi nước tạo ra axit nitric
5. Mở rộng kiến thức về NO2 (nitơ đioxit)
Khí NO2 là gì?
Công thức hóa học: NO2.
Khí NO2 hay có tên gọi khác là nitrit, khí nitơ đioxit hay điôxít nitơ. Nó là một trong các loại oxit nito.
Khí NO2 có màu nâu đỏ có mùi gắt rất đặc trưng. Vì thế khí NO2 có mùi dễ nhận biết hơn so với các khí độc khác và dễ dàng phát hiện ra nếu có rò rỉ.
Tính chất hóa học của NO2
NO2 tham gia vào phản ứng oxy hóa khử:
3NO2 + H2O → 2HNO3 + NO
(Trong phản ứng này ta thấy NO2 vừa là chất oxy hóa vừa là chất khử).
NO2 tham gia vào phản ứng quang hóa trong điều chế NO
NO2 + hv (λ < 430 nm) → NO + O
6. Bài tập vận dụng liên quan
Câu 1. Quá trình nào dưới đây không làm giảm lượng oxi trong không khí?
A. Sự gỉ của các vật dụng bằng sắt ngoài không khí
B. Sự quang hợp của cây xanh trong tự nhiên
C. Sự cháy của than, củi, bếp ga
D. Sự hô hấp của động vật con người
Đáp án B
Câu 2. Trong công nghiệp bằng cách nào sau đây để sản xuất khí nitơ?
A. Chưng cất phân đoạn không khí lỏng
B. Nhiệt phân NH4NO3
C. Dùng phương pháp dời nước
D. Nhiệt phân muối amoni clorua NH4Cl
Đáp án A
Câu 3. Nhỏ từ từ dung dịch NH3 cho đến dư vào ống nghiệm đựng sẵn dung dịch Al2(SO4)3. Hiện tượng quan sát được trong quá trình phản ứng là:
A. Có kết tủa keo trắng xuất hiện, sau đó kết tủa lại tan dần
B. Có kết tủa keo màu trắng xuất hiện
C. Có kết tủa màu xanh lục xuất hiện, sau đó kết tủa lại tan dần
D. Có kết tủa màu xanh lục xuất hiện
Đáp án B
6NH3 + Al2(SO4)3 + 6H2O → 2Al(OH)3 + 3(NH4)2SO4
Xuất hiện kết tủa trắng
Câu 4. Oxit phi kim nào dưới đây không phải là oxit axit?
A. CO2
B. N2O5
C. P2O5
D. NO
Đáp án D
Câu 5. Dãy kim loại nào dưới đây không phản ứng với HNO3 đặc nguội
A. Al, Zn, Fe
B. Al, Cr, Fe
C. Cu, Ag, Cr
D. Cu, Cr, Fe
Đáp án B
Câu 6. Khí nào dưới đây gây ra hiện tượng mưa axit?
A. H2
B. NH3
C. CH4
D. SO2
Đáp án D
Câu 7. Trong phòng thí nghiệm, người ta điều chế HNO3 từ?
A. NH3 và O2
B. NaNO3 và H2SO4 đặc
C. NaNO3 và HCl đặc
D. NaNO2 và H2SO4 đặc.
Đáp án B: NaNO3tinh thể và H2SO4đặc NaHSO4 + HNO3
Câu 8. Đem nung hỗn hợp A gồm: x mol Fe và 0,15 mol Cu, trong không khí một thời gian, thu được 63,2 gam hỗn hợp B, gồm hai kim loại trên và hỗn hợp các oxit của chúng. Đem hòa tan hết lượng hỗn hợp B trên bằng dung dịch HNO3 đậm đặc, thì thu được 0,6 mol NO2. Trị số của x là:
A. 0,7 mol
B. 0,6 mol
C. 0,5 mol
D. 0,4 mol
Đáp án A
nO = y mol; nFe = x mol
56x + 0,15.64 + 16y = 63,2 (1);
3x + 0,15.2 = 2y + 0,6 (2)
Từ 1, 2 → x = 0,7 và y = 0,9
Câu 9. Đốt cháy 11,2 gam bột Fe trong bình đựng O2 thu được 14,72 gam hỗn hợp X gồm Fe2O3, Fe3O4 và Fe. Hòa tan hoàn toàn lượng hỗn hợp X bằng dung dịch HNO3 thu được V lít hỗn hợp khí Y gồm NO và NO2. Tỉ khối của B so với H2 bằng 19. Thể tích V ở đktc là:
A. 1792 ml
B. 672 ml.
C. 448 ml.
D. 896 ml.
Đáp án A
MX = 19.2 = 38
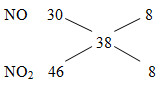
→ nN2 = nNO2 = x
mFe + mO = moxit
→ mO = moxit – mFe = 14,72 – 11,2 = 3,52 gam
→ nO = 0,22 mol
Fe0 → Fe3+ + 3e
0,2 → 0,6
O0 + 2e →O2-
0,22 → 0,44
N+5 + 3e → N+2
3x x
N+5 +1e → N+4
x x
Bảo toàn e: 0,6 = 0,44 + 3x + x =0,44+4x → x= 0,04
→ nkhí = 2x = 0,08 mol
→ Vkhí = 0,08.22,4 = 1,792 lít = 1792 ml
Câu 10. Cho 30 gam hỗn hợp X gồm: Fe; FeO; Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư được 5,6 lít khí NO (đktc, sp khử duy nhất) và dung dịch Y. Số mol của HNO3 đã phản ứng là:
A. 1 mol
B. 1,45 mol
C. 1,6 mol
D. 1,35 mol
Đáp án C
Quy đổi 30 gam hỗn hợp X thành Fe, và O. Gọi x, y lần lượt là số mol của Fe và O →
56x + 16y = 30 (1);
3x – 2y = 0,25.3 (2);
Từ 1, 2 → x = 0,45 và y = 0,3; nHNO3 = 4.nNO + 2nO = 4.0,25 + 2.0,3 = 1,6 mol
Câu 11. Chỉ dùng H2O và điều kiện đun nóng có thể tách hổn hợp nào sau đây?
A. NH4Cl, K2CO3, KCl
B. NH4NO3, CaCO3, Na2SO4
C. NH4Cl, CaSO4, MgSO4
D. Tất cả đều thực hiện được
Đáp án C
Câu 12. Cho 150 ml dung dịch KOH 1M tác dụng với 200 ml dung dịch H3PO4 0,5M. Sau phản ứng, trong dung dịch chứa các muối
A. KH2PO4 và K2HPO4.
B. KH2PO4 và K3PO4.
C. K2HPO4 và K3PO4.
D. KH2PO4, K2HPO4 và K3PO4
Đáp án A
Câu 13. Cho kim loại Cu tác dụng với HNO3 đặc hiện tượng quan sát được là :
A. Khí màu nâu bay lên, dung dịch chuyển màu xanh
B. Khí không màu bay lên, dung dịch chuyển màu xanh
C. Khí không màu bay lên, dung dịch có màu nâu
D. Khí thoát ra không màu hoá nâu trong không khí, dung dịch chuyển sang màu xanh
Đáp án A
Câu 14. Hòa tan hết m gam FeS bằng một lượng tối thiểu dung dịch HNO3 (dung dịch X), thu được dung dịch Y và khí NO. Dung dịch Y hòa tan tối đa 1,92 gam Cu. Biết trong các quá trình trên, sản phẩm khử duy nhất của N+5 đều là NO. Số mol HNO3 trong X là
A. 0,48.
B. 0,12.
C. 0,36.
D. 0,24.
Đáp án D
nCu = 0,03 mol
Ta có: 2Fe3+ + Cu → 2Fe2+ + Cu2+
→ nFe3+(Y) =0,6 mol → nFeS = 0,6 mol
FeS → Fe3+ + S+6 + 9e
N+5 + 3e → N+2
→ Bảo toàn e: nNO =3.nFe3+ = 0,18 mol
Dung dịch Y chứa Fe2(SO4)3 và Fe(NO3)3
Bảo toàn nguyên tố S: nFe2(SO4)3 =1/3.nFeS = 0,02 mol
Bảo toàn nguyên tố Fe và S :
nFeS = 2.nFe2(SO4)3 + nFe(NO3)3
→ nFe(NO3)3= 0,06 − 2.0,02 = 0,02 → nNO − 3nNO3− muối = 0,06 mol
Bảo toàn nguyên tố N: nHNO3 = nNO + nNO3−muối = 0,36 + 0,12 = 0,24 mol
………………………….
Trường Cao đẳng nghề Thừa Thiên Huế đã gửi tới bạn phương trình hóa học NO2 + O2 + H2O → HNO3. Với phương trình hóa học này các em lưu ý chất tham ra cần có O2 và H2O thì NO2 mới tạo ra được axit nitric HNO3. Chúc các bạn học tập tốt.
Mời các bạn tham khảo một số tài liệu liên quan:
Trên đây Trường Cao đẳng nghề Thừa Thiên Huế vừa giới thiệu tới các bạn phương trình hóa học NO2 + O2 + H2O → HNO3, mong rằng qua bài viết này các bạn có thể học tập tốt hơn môn Hóa lớp 12. Mời các bạn cùng tham khảo thêm các môn Ngữ văn 12, Tiếng Anh 12, Thi thpt Quốc gia môn Toán, Thi THPT Quốc gia môn Vật Lý,….
Ngoài ra, Trường Cao đẳng nghề Thừa Thiên Huế đã thành lập group chia sẻ tài liệu học tập THPT miễn phí trên Facebook: Tài Liệu Học Tập Trường Cao đẳng nghề Thừa Thiên Huế . Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
Chúc các bạn học tập tốt.